La protéine KR2 [1] transporte les ions sodium chargés positivement hors de la cellule, une faculté que les chercheurs en optogénétique ne parviennent pas à exploiter. Jusqu’à présent, la structure atomique et le mécanisme d’action de KR2 n’étaient pas connus. Ce défi, les chercheurs de l’Institut de biologie structurale (CEA/CNRS/Université Joseph Fourier, Grenoble), du Moscow Institute of Physics and Technology (Russie) et de l’Institute of Complex Systems (Forschungszentrum Jülich, Allemagne) l’ont relevé en utilisant des techniques de cristallographie à rayons X. Ils ont ainsi obtenu la reconstitution 3D exacte de la structure atomique de KR2, ainsi que la structure du complexe moléculaire qu’elle forme en conditions physiologiques – en effet, dans notre organisme, la protéine KR2 s’associe à quatre autres KR2 pour former un complexe moléculaire pentamérique.
La structure de KR2 présente des caractéristiques originales, dont une partie hélicoïdale recouvrant l’entrée extracellulaire de la pompe, comme un couvercle. Une caractéristique qui intéresse particulièrement les chercheurs est la structure inhabituelle de la cavité de chargement des ions du côté intracellulaire. Elle est inhabituellement large et en protrusion dans le cytoplasme par rapport à la surface de la membrane. Cette structure pourrait agir comme un filtre à l’origine de la sélectivité de KR2 pour les ions sodium.
Pour tester cette hypothèse, les chercheurs ont modifié la structure de ce « filtre » en changeant les acides aminés spécifiques de ce site moléculaire par mutations ciblées. Non seulement KR2 perd effectivement sa compétence vis-à-vis des ions sodium, mais une de ces mutations transforme KR2 en pompe à potassium photosensible – une première du genre.
Une série de tests effectuée au Max Planck Institute of Biophysics (Francfort, Allemagne) a confirmé cette observation.
Ces résultats sont particulièrement intéressants pour des applications potentielles en optogénétique : un neurone activé revient normalement à un état de repos en laissant sortir des ions potassium à travers des canaux ioniques dans sa membrane. Une pompe potassium KR2 mutée pourrait être utilisée pour « éteindre » à volonté, grâce à des impulsions lumineuses, un neurone actif. Elle constituerait alors un système de contrôle précis à disposition des chercheurs.
Les auteurs de l’étude travaillent maintenant au développement d’une méthode d’intégration par transfection [2] de ce système dans différents types de neurones, et notamment à l’amélioration de l’adressage de ces protéines dans la membrane plasmique des neurones transfectés.
À propos de l’usage des pompes ioniques en neurosciences et de l’optogénétique
Les neurones sont parcourus par les influx nerveux, messages électriques à l’origine de toutes les pensées et actions. Ces messages résultent du transport de certains ions à travers leur membrane plasmique, rendus possibles grâce à des protéines particulières (pompes et canaux ioniques). Les neurones ne sont pas les seules cellules à posséder de telles protéines. Particularité chez certains organismes, elles peuvent être photosensibles, c’est-à-dire qu’elles sont activées par la lumière (famille des opsines). C’est le cas de KR2 qui transporte les ions sodium chargés positivement hors de la cellule.
Intégrer ces transporteurs d’ions dans la membrane des neurones permet d’agir sur leur état de charge en utilisant des impulsions lumineuses, rendant possible le contrôle de leur activité avec précision : c’est l’optogénétique. Par ce procédé, Les chercheurs peuvent « stopper » l’activité d’un neurone, permettant d’étudier le fonctionnement de réseaux de neurones in vitro, ex vivo (tranches de cerveau), voire même in vivo. Cette méthode a rapidement été utilisée en neurosciences, mais seul un nombre limité de telles protéines est aujourd’hui disponible. Augmenter leur diversité en jouant notamment sur la sélectivité des ions transportés est une attente forte des chercheurs.
Schéma de la structure moléculaire de KR2 et du complexe qu'elle forme. La pompe KR2 est constituée de sept hélices transmembranaires à travers lesquelles les ions sodium sont transportés. Une courte hélice supplémentaire (bleu), structure originale chez les pompes ioniques photosensibles, couvre l'ouverture extérieure de la pompe, comme un couvercle. L'activité de pompage est contrôlée par une petite molécule photosensible, le rétinal (vert). © Research Center Jülich/IBS Grenoble.
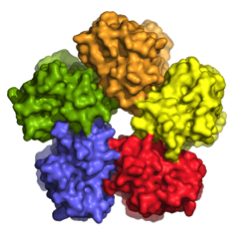
En condition physiologique, cinq molécules KR2 s’associent spontanément en complexe en forme d’étoile. © Research Center Jülich/IBS.
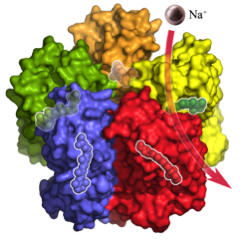 |  |
La surface du complexe KR2 vue de côté. Chacune des cinq molécules KR2 se lie et transporte un ion sodium (violet) à travers la membrane. Le rétinal photosensible à l’intérieur du complexe, qui régule l’activité de pompage, est représenté en superposition transparente. © Research Center Jülich/IBS Grenoble
[1] En 2013, des scientifiques travaillant sur la bactérie marine Krokinobacter eikastus ont découvert, dans la membrane de cette bactérie, une protéine servant de transporteur d’ion et de type inconnu. Baptisée KR2, elle appartient à un groupe de protéines devenues les piliers de la recherche « optogénétique » : exposées à la lumière, cette famille de protéines permet, en transportant des particules chargées à travers la membrane cellulaire, de modifier le potentiel électrique des cellules.
[2] Processus de transfert de gènes, c'est-à-dire l'introduction directe de matériel génétique dans des cellules.